Métastase pariétale abdominale d´un cancer de l´endomètre: une localisation inhabituelle (à propos d´un cas)
Ayoub Khtira, Hamza Messaoudi, Moad Belouad, Jaouad Kouach
Corresponding author: Ayoub Khtira, Service de Gynécologie Obstétrique, Hôpital Militaire d´Instruction Mohammed V, Rabat, Maroc 
Received: 06 Aug 2023 - Accepted: 27 Sep 2023 - Published: 12 Oct 2023
Domain: Gynecology
Keywords: Cancer de l´endomètre, risque intermédiaire, curiethérapie, métastase, cas rapporté
©Ayoub Khtira et al. PAMJ Clinical Medicine (ISSN: 2707-2797). This is an Open Access article distributed under the terms of the Creative Commons Attribution International 4.0 License (https://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Cite this article: Ayoub Khtira et al. Métastase pariétale abdominale d´un cancer de l´endomètre: une localisation inhabituelle (à propos d´un cas). PAMJ Clinical Medicine. 2023;13:13. [doi: 10.11604/pamj-cm.2023.13.13.41346]
Available online at: https://www.clinical-medicine.panafrican-med-journal.com//content/article/13/13/full
Case report 
Métastase pariétale abdominale d´un cancer de l´endomètre: une localisation inhabituelle (à propos d´un cas)
Métastase pariétale abdominale d'un cancer de l'endomètre: une localisation inhabituelle (à propos d'un cas)
Abdominal wall metastasis of endometrial carcinoma: an unusual location (case report)
![]() Ayoub Khtira1,&, Hamza Messaoudi1,
Ayoub Khtira1,&, Hamza Messaoudi1, ![]() Moad Belouad1, Jaouad Kouach1
Moad Belouad1, Jaouad Kouach1
&Auteur correspondant
La paroi abdominale est une localisation rare des métastases du cancer de l'endomètre. Nous rapportons le cas d'une patiente de 66 ans qui s'est présentée avec une masse inflammatoire volumineuse sur la paroi abdominale antérieure. Elle avait bénéficié 5 mois auparavant d'une hystérectomie totale avec annexectomie bilatérale pour un adénocarcinome endométrioïde de l'endomètre de stade de la Fédération Internationale de Gynécologie et d'Obstétrique (FIGO) IB. Une résection chirurgicale de la masse pariétale a été réalisée et l'examen anatomo-pathologique a révélé un processus carcinomateux de mêmes caractéristiques que l'origine endométriale connue de la patiente. Elle bénéficie actuellement d'une chimiothérapie à visée palliative. La localisation pariétale abdominale est une localisation métastatique à ne pas méconnaitre dans le cancer de l'endomètre. Sa présentation clinique peut mimer un hématome de paroi. La radiothérapie post-opératoire diminue le risque de récidive loco-régionale.
The abdominal wall is a rare site for endometrial cancer metastases. We report the case of a 66-year-old female patient who presented with voluminous inflammatory mass arising from the anterior abdominal wall. She had undergone total hysterectomy with bilateral adnexectomy for International Federation of Gynecology and Obstetrics (FIGO) stage IB endometrioid adenocarcinoma 5 months before. Surgical resection of the wall mass was performed and anatomo-pathological examination showed a carcinomatous process having the same characteristics as endometrioid adenocarcinoma known to the patient. She is currently receiving palliative chemotherapy. Abdominal wall can be a metastases site and this should not be ignored in the management of patients with endometrial cancer. Its clinical presentation may mimic wall hematoma. Postoperative radiotherapy reduces the risk of loco-regional recurrence.
Key words: Endometrial cancer, intermediate risk, brachytherapy, metastasis, case report
Le cancer de l'endomètre est le cancer gynécologique pelvien le plus fréquent dans les pays développés, et son incidence est en nette augmentation. Il survient généralement chez les femmes ménopausées bien que 20% soit diagnostiqués avant la ménopause [1]. Il est généralement détecté à un stade précoce et se manifeste par des saignements utérins anormaux, le plus souvent des métrorragies post-ménopausiques [2]. L'hystéroscopie diagnostique permet de réaliser des biopsies endométriales dont l'examen anatomopathologique pose le diagnostic. Le type histologique le plus fréquent est le carcinome endométrioïde (80%). Il est œstrogéno-dépendant. Il est subdivisé, selon l'OMS (Organisation Mondiale de la Santé), en 3 grades: grade 1 (bien différencié), grade 2 (moyennement différencié), et grade 3 (peu différencié). L'imagerie par résonnance magnétique (IRM) pelvienne et lombo-aortique est le gold standard pour le bilan d'extension. Elle permet d'apprécier le volume tumoral, le pourcentage d'infiltration du myomètre, la présence d'adénopathies pelviennes et lombo-aortiques, l'atteinte du col, des annexes, du vagin, de la vessie et du rectum. La prise en charge thérapeutique dépend du stade FIGO (Fédération Internationale de Gynécologie et d'Obstétrique) et de l'évaluation du risque. Nous présentons le cas d'une patiente de 66 ans, suivie pour un carcinome endométrioïde de stade IB FIGO de risque intermédiaire, qui a présenté, 5 mois après une hystérectomie totale avec annexectomie bilatérale, une récidive métastatique au niveau de la paroi abdominale antérieure.
Informations relatives à la patiente: il s'agit d'une patiente âgée de 66 ans, nulligeste, hypertendue, obèse (indice de masse corporelle = 42 kg/m²), et ménopausée depuis 10 ans. Elle n'a aucun antécédant familial de cancer. Elle a consulté initialement pour un saignement utérin anormal à type de métrorragies post-ménopausiques de petite abondance, sans autres signes associés gynécologiques ou extra-gynécologiques.
Résultats cliniques: l'examen clinique à l'admission retrouve une patiente en bon état général, conjonctives normo-colorées, tension artérielle à 139/85 mmHg, fréquence cardiaque à 85 battements par minute, pesant 108 kg et mesurant 160 cm (IMC = 42 kg/m²), avec une température à 36,7°C. Les examens sénologique et abdominal sont normaux. L'examen gynécologique retrouve au speculum un col d'aspect sain avec des stigmates de saignement noirâtre, et au toucher vaginal un utérus augmenté de taille à un travers de doigt au-dessus de la symphyse pubienne, sans masse latéro-utérine palpable.
Démarche diagnostique: une échographie pelvienne a été réalisée, montrant un utérus augmenté de taille (12 x 8 x 6 cm), polymyomateux (dont le plus volumineux mesure 4 cm de grand axe, corporéal postérieur de type 2-5 FIFO), avec une hypertrophie endométriale mesurée à 12 mm, associée à une image intracavitaire hyperéchogène hypervascularisée au doppler, suspecte. L'hystéroscopie diagnostique a montré un processus ulcéro-bourgeonnant de localisation corporéale antérieure, saignant au contact. Une biopsie dirigée a été réalisée dont l'examen anatomopathologique est revenu en faveur d'un adénocarcinome endométrioïde de grade 1 de l'OMS. Dans le cadre du bilan d'extension, une IRM pelvienne et lombo-aortique a été réalisée et a révélé un processus endométrial infiltrant plus de 50% du myomètre, respectant le col utérin, les annexes, le vagin et les paramètres, avec absence d'adénopathies pelviennes et lombo-aortiques. La tumeur a été classée stade IB selon la classification de FIGO de 2018 et de risque intermédiaire.
Intervention thérapeutique: la patiente a bénéficié d'une hystérectomie totale avec annexectomie bilatérale suite à la décision du staff de réunion de concertation pluridisciplinaire (RCP). L'intervention chirurgicale a été réalisée par laparoscopie, avec conversion en laparotomie devant la difficulté technique à extraire la pièce opératoire par voie vaginale étant donné l'utérus volumineux. Ainsi, la pièce d'hystérectomie totale avec annexectomie bilatérale a été extraite par une incision de type Pfannenstiel.
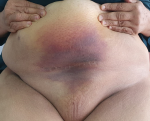
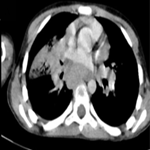
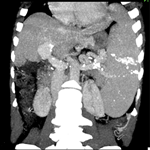
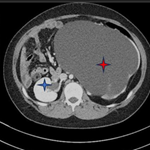
Suivi et résultats des interventions thérapeutiques: l'examen anatomopathologique de la pièce opératoire retrouve un adénocarcinome endométrioïde de grade 1 de l'OMS infiltrant 60% du myomètre, classé pT1b. Le col utérin, les trompes et les ovaires sont indemnes de lésion néoplasique, avec absence d'emboles vasculaires. Devant le risque intermédiaire bas, la décision du staff RCP était de réaliser une curiethérapie vaginale post-opératoire. La patiente a été adressée au service de radiothérapie. Cependant, elle a été perdue de vue pour des raisons familiales et consulte à 5 mois du post-opératoire pour douleur abdominale. L'examen physique retrouve une masse hypogastrique inflammatoire (Figure 1), évoquant un hématome pariétal ou une récidive métastatique pariétale. Un scanner de tomographie par émission de positons (TEP) (Figure 2) a été réalisé retrouvant deux volumineuses masses pariétales pelviennes contiguës de fixation très intense et très hétérogène, la plus volumineuse est pelvienne gauche, mesurant 12 x 10 cm à centre amétabolique et à circonférence hyperfixante, la 2e est médiane, mesurant 8 x 6 cm, de mêmes caractéristiques.
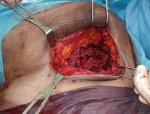
La patiente a bénéficié d'une seconde intervention chirurgicale avec reprise de l'ancienne cicatrice de Pfannenstiel. L'exploration après incision cutanée retrouve une masse rougeâtre friable infiltrant le muscle grand droit de l'abdomen et son aponévrose (Figure 3). Une exérèse non carcinologique de la masse pariétale a été réalisée, sans ouverture du péritoine. L'examen anatomo-pathologique retrouve une localisation pariétale d'un processus carcinomateux peu différencié compatible avec l'origine endométriale connue chez la patiente. Après décision du staff de RCP, la patiente suit actuellement un protocole de chimiothérapie palliative associant paclitaxel et carboplatine.
Perspectives du patient: la patiente approuve les traitements reçus.
Consentement éclairé: la patiente a donné son consentement éclairé pour la publication de ce travail.
La prise en charge du cancer de l'endomètre est basée sur l'évaluation du risque. Pour notre patiente, il s'agit d'un carcinome endométrioïde classé initialement de risque intermédiaire (stade IB FIGO de grade 1 de l'OMS), indiquant une hystérectomie totale avec salpingo-ovariectomie bilatérale. La stadification post-chirurgicale a conclu un risque intermédiaire bas (stade IB de grade 1 avec absence d'emboles vasculaires). Devant le risque intermédiaire bas, il est recommandé de réaliser une curiethérapie post-opératoire. La curiethérapie a une place importante dans la stratégie thérapeutique car elle diminue le risque de récidive loco-régionale. En effet, le taux de récidive locorégionale est de 4 à 20%, réduit de 0 à 5% après curiethérapie postopératoire du fond vaginal [3]. Notre patiente a été perdue de vue après la chirurgie et n'a justement pas bénéficié de cette curiethérapie.
Les récidives du cancer de l'endomètre sont le plus souvent localisées dans le vagin, les ganglions lymphatiques pelviens et lombo-aortiques, le péritoine, les poumons et le foie. Les sites inhabituels comprennent la paroi abdominale antérieure (2 à 6%), la rate (1%), le système nerveux central (< 1%), les ganglions lymphatiques extra-abdominaux (0,4 à 1%) et, plus rarement, appendice, surrénales et pancréas [4]. Les mécanismes métastatiques sur la paroi abdominale antérieure ne sont pas clairement élucidés. Les métastases de la paroi abdominale antérieure ont principalement été associées à l'incision chirurgicale, que ce soit par laparotomie ou laparoscopie [5]. En effet, le principal mécanisme suggéré serait l'ensemencement direct des cellules néoplasiques sur la paroi abdominale antérieure lors de l'extériorisation de la pièce opératoire [6].
Par ailleurs, la paroi abdominale antérieure possède une vascularisation artérielle riche, un réseau veineux anastomotique, et un système lymphatique qui se draine crânialement et caudalement vers plusieurs chaînes lymphatiques. Tous ces systèmes pourraient être impliqués dans la dissémination des cellules néoplasiques vers la paroi abdominale antérieure, par voie hématogène ou lymphatique [7].
Ce cas met en évidence d'une part la localisation métastatique inhabituelle du cancer de l'endomètre sur la paroi abdominale antérieure et d'autre part l'intérêt de la curiethérapie vaginale post-opératoire dans la diminution du risque de récidive loco-régionale.
Les auteurs ne déclarent aucun conflit d'intérêts.
Tous les auteurs ont contribué à la prise en charge diagnostique et thérapeutique de cette patiente. Ayoub Khtira a rédigé le manuscrit. Tous les auteurs ont lu et approuvé la version finale du manuscrit.
Figure 1: vue antérieure de la paroi abdominale montrant un placard cutané inflammatoire en regard de l'hypogastre
Figure 2: scanner de tomographie par émission de positons en coupe transversale à l'étage pelvien montrant deux masses pariétales pelviennes contiguës de fixation intense et hétérogène à centres amétaboliques, la plus volumineuse est pelvienne gauche mesurant 12 x 10 cm (flèche pleine), la 2e est médiane mesurant 8 x 6 cm (flèche en pointillés)
Figure 3: vue per-opératoire de la paroi abdominale antérieure montrant une masse rougeâtre friable adhérente au muscle grand droit de l'abdomen et à son aponévrose
- Siegel RL, Miller KD, Jemal A. Cancer statistics, 2016. CA Cancer J Clin. 2016 Jan-Feb;66(1):7-30. PubMed
- American Joint Committee on Cancer. Corpus Uteri. In: AJCC Staging manual. 7th Edition. New York: Springer, 2010.
- Peiffert D, Hoffstetter S, Charra-Brunaud C. Curiethérapie des cancers de l'endomètre. Cancer/Radiothérapie. 2003;7(2):121-131. Google Scholar
- Kurra V, Krajewski KM, Jagannathan J, Giardino A, Berlin S, Ramaiya N. Typical and atypical metastatic sites of recurrent endometrial carcinoma. Cancer Imaging. 2013 Mar 26;13(1):113-22. PubMed | Google Scholar
- Palomba S, Falbo A, Oppedisano R, Russo T, Zullo F. Isolated port-site metastasis after laparoscopic surgery for endometrial cancer: A case report. Gynecol Oncol Case Rep. 2011 Dec 2;2(1):16-7. PubMed | Google Scholar
- Macias V, Baiotto B, Pardo J, Muñoz F, Gabriele P. Laparotomy wound recurrence of endometrial carcinoma. Gynecol Oncol. 2003 Nov;91(2):429-34. PubMed | Google Scholar
- Luz R, Leal R, Simões J, Gonçalves M, Matos I. Isolated abdominal wall metastasis of endometrial carcinoma. Case Rep Obstet Gynecol. 2014;2014:505403. PubMed | Google Scholar
Search
This article authors
On Pubmed
On Google Scholar
Citation [Download]
Navigate this article
Similar articles in
Key words
Tables and figures
 Figure 2: scanner de tomographie par émission de positons en coupe transversale à l'étage pelvien montrant deux masses pariétales pelviennes contiguës de fixation intense et hétérogène à centres amétaboliques, la plus volumineuse est pelvienne gauche mesurant 12 x 10 cm (flèche pleine), la 2e est médiane mesurant 8 x 6 cm (flèche en pointillés)
Figure 2: scanner de tomographie par émission de positons en coupe transversale à l'étage pelvien montrant deux masses pariétales pelviennes contiguës de fixation intense et hétérogène à centres amétaboliques, la plus volumineuse est pelvienne gauche mesurant 12 x 10 cm (flèche pleine), la 2e est médiane mesurant 8 x 6 cm (flèche en pointillés)